锂电池开发史(二)LiCoO2与碳胜出,为回避专利绞尽脑汁
2015-03-12 08:41:23 腾讯科技 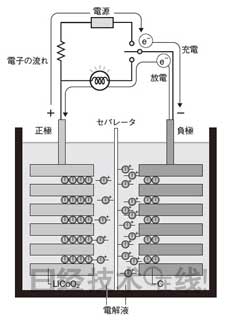 |
| 图1:LIB的基本原理 正极(LiCoO2)与负极(C)之间通过交换Li+离子进行充放电。 (点击放大) |
图1是LIB充放电机制的模式图。其重点在于正极(这里是LiCoO2)与负极(石墨)都如图所示,为层状结构。
通常的二次电池在充放电过程中会发生氧化还原反应,也就是化学反应。比方说,Ni-Cd二次电池在充电时,正极发生氧化,从Ni(OH)2转变为NiOOH,在负极,Cd(OH)2还原为Cd(镉)。放电则相反,NiOOH还原为Ni(OH)2,镉氧化为Cd(OH)2。
但LIB不发生这样的氧化还原反应。充电时,正极层间的锂离子(Li+)移动到负极层间,也就是“搬家”,除此之外再没有其他现象。放电时,负极层间的Li+移动到正极层间。充放电不伴随任何化学反应,只是Li+在二者之间搬来搬去而已。简直就是现实版的“三轩长屋”。因为离子在两个位置间反复来回,所以LIB之类的电池也叫作“摇椅型电池”(但却没有三轩长屋型电池的说法)。
那么,我们是怎么发现这一机制的?这要先来回顾索尼的开发轨迹。
通过比赛选择电极材料
从1980年代中期开始,二次电池的需求与日俱增。当时,索尼集团旗下拥有电池制造企业——索尼能源技术(SET,现在的索尼能源设备),但该公司的强项在于碱性干电池和氧化银电池等,并不生产二次电池。市场对于二次电池的需求愈发强烈。因此,开发小型、大容量的二次电池成为了SET这家电池企业的当务之急。
但索尼在二次电池领域完全是新军,要想迎头赶上,就必须加快开发速度。为此,索尼采取了以下策略。
① 任命SET的高管担任二次电池开发项目的主管。这样一来,决定重要事项无需再一一提交申请书,加快了各项事务的决策速度。
② 试制装置和测量仪等的数量准备需要数量的几倍。倘若仪器只有1台,一旦发生故障,在修理期内将无法使用,会阻碍开发的进行。准备两台可以避免耽误时间。
③ 材料(正极材料、负极材料和电解液等)的库存也必须达到需要量的2倍以上。因为如果某一种材料发生短缺,在订购到交货期间只能束手无策。
但其中最为关键的,还是为开发目标——电池确定结构。电池的组件中,直接关系到发电的是正极活性物质、电解液和负极活性物质三种。三要素的组合据说多达约1亿1000种。
那么,实际投入实用的电池有多少种?笔者没有细数,大致推算估计在30种左右。也就是说,在可能存在的组合中,只有0.3ppm投入了实用。实用化率如此之低,原因究竟何在?
当然,很多组合并不具备足够的性能。但在笔者看来,开发电池最重要、最困难的课题,是有效而且安全地在有限的电池筒内集合上面的三要素。比如说,在筒内封闭氢气很难,但镍氢(Ni-MH)电池借助贮氢合金使之成为可能,成功实现了二次电池化。我们已经下定决心要发展锂电池。但包括使用什么锂化合物可以良好地在筒中收纳、正极采用什么材料、什么能够用作电解液在内,需要研究的难题还比比皆是。为此,索尼在上述①~③项开发加速策略的基础上,又补充了第四个项目。
④ 并行推动多个构想,最后筛选出一个。也就是以比赛的形式进行开发,让表现好的选手胜出。
金属锂作为负极虽然潜力巨大,但枝晶问题使其很难应用于二次电池。鉴于此,我们当时的想法,是使用锂与其他金属的合金。
例如,铝与锂组成的合金配比多种多样。使用这样的合金作为负极,在放电时,铝合金中的锂将发生离子化,释放出电子,在充电时,锂离子将回到铝合金中,能够构成摇椅型电池。这是不是意味着锂二次电池具备了实用化的条件?事情没有这么简单。
这种电池会在短暂的充放电循环中出现功能障碍,放电深度(DOD)*必须非常浅。DOD=20%时,寿命的极限为50个循环左右,DOD=15%时也仅为100个循环左右。改善循环特性必须进一步缩小DOD,锂的能量只有极小部分能够使用。
*放电深度(DOD)=放电量与额定容量的比例。一般来说,放电深度越浅,电池的寿命越长。DOD是depth of discharge的缩写。
我们尝试利用许多不同的正极、负极材料持续试制电池,为众多试制品进行了编号。编号的规则如下:负极材料A与正极A1组成的电池的编号为US-11,负极为A,正极改换A2的电池编号为US-12。US是Ultra Super的缩写。负极改换物质B时,以US-21为起始,按照US-22、US-23的顺序编号。
举例来说,上面提到的负极使用铝与锂的合金(Al-Li),正极使用锰(Mn)系材料的电池编号为US-41。因为US-41已经证明了Al-Li负极的DOD浅,无法实际应用,所以US-42之后的编号全部空缺。
经过不懈地试制,编号为US-61的试制品成为了开发大赛的赢家。US-61以碳(C)为负极,LiCoO2为正极,最终成长为了日后的LIB。
难产的LIB呱呱坠地
随着US-61赢得开发大赛,开发的目标锁定在了正极采用LiCoO2、负极采用碳的系统。
但这种系统必须要解决负极使用哪种碳最好的问题。碳的形态多种多样,有石墨、软碳、硬碳(HC),还有金刚石(图2)。除了金刚石之外,其他任何一种都可以作为负极。
 |
| 图2:能够成为负极的碳 石墨的六方晶晶体排列整齐。软碳的微小晶体比较整齐,但加热后容易转变为石墨。硬碳的微小晶体排列混乱,但加热后不转变为石墨。 |
而且,经过查阅资料,使用碳和锂的化合物作为负极的技术其实早已有之。就笔者所知,最古老的相关专利是德国莱茵集团(Rheinisch-Westfalisches ElektrizitatswerkAG)于1978年申请的“DE 2834 485 C2”(H.P. Fritz等,1978年8月7日申请,1980年2月14日公开)。上面明确记载,使用铝和锂的合金作为负极的二次电池可以用碳替代铝。
其次,美国宾夕法尼亚大学(University of Pennsylvania)的A.G. MacDiarmid等人申请的专利(1980年3月11日申请,1982年3月23日注册)也宣布包含C-Li负极的概念。MacDiarmid曾凭借发现导电性聚合物——聚乙炔荣获诺贝尔奖,这项专利提出了“在具有共轭双键的聚合物(以聚乙炔为代表)中插入锂后作为负极的电池”的构想注2)。他们主张石墨也是具有共轭双键的聚合物,因此,石墨与锂组成的负极也属于他们的专利。如何回避这些专利成了一道难题。
注2) 共轭双键是指两个以上的双键隔着一个单键排列的化学结合。苯是由三个双键和三个单键交替结合形成的六角形化合物,石墨由苯环的碳骨架组成。因此发明者主张石墨也是具有共轭双键的化合物。
而且,碳为电化学惰性物质,很难单独作为负极。虽然可以与锂组成合金,但安全地工业化生产碳和锂的化合物存在困难注3)。
注3) 锂与碳的化合物的合成方法包括在高温真空下蒸发金属锂,使锂与碳发生反应,或是使特殊的锂有机化合物与碳在有机溶剂中发生反应,这些方法都伴随复杂的工序,而且成本高昂。
那么,不含锂的碳怎样才能单独作为负极?当时的一个构想,是开发让正极一侧含锂,在充电时,锂从正极向负极的碳移动的系统。有没有化合物含锂,而且能够通过电化学反应,自由地释放、吸收锂?
其实,SET在1980年申请了与化合物AgNiO2相关的专利(图3)。开发这种化合物原本是为了作为氧化银电池的正极。AgNiO2的NiO2层之间插入了银(Ag),银具有在在层间自由出入的性质。
 |
| 图3:SET申请的AgNiO2相关专利 1980年6月为电极材料使用AgNiO2的碱性电池申请专利。 (点击放大) |
既然如此,在层间用锂取代银的化合物——LiNiO2也有可能成为锂离子可以脱离并重新插入的化合物。而且,钴(Co)的性质与镍(Ni)类似,LiCoO2说不定也能成为正极的候选材料。通过灵活利用AgNiO2的专利,在知识产权上或许可以掌握有利的局面。我们的期待顿时膨胀了起来。
然而,经过调查,我们发现了使用LiNiO2作为电极的专利(图4)。内容正是我们所设想的正极化合物。而且,在发明者一栏,罗列着J.B Goodenough(足够优秀)、P.J Wiseman(贤者)等单从字面上就仿佛预示我们将要败北的名字。申请日期是1980年4月3日,只比索尼的AgNiO2专利(1980年6月4日申请)早2个月。我们原本还在想“就差2个月啊,真遗憾”,定睛一看,这项专利还附注了追溯到1979年4月5日的优先权声明*。
*优先权声明=在某国申请专利的1年内,在别国申请相同专利时,可以依据最初提出申请的国家的申请日,主张新颖性、进步性和先使用权。这项规定在1883年的巴黎条约上商议通过,在该条约的成员国之间有效。
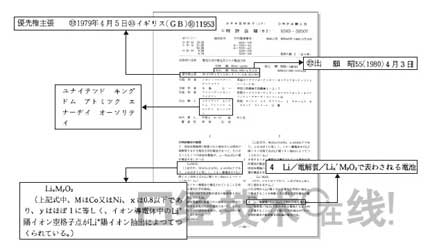 |
| 图4:Goodenough等人在1980年4月申请的专利 电极材料使用LiCoO2和LiNiO2的电化学电池的专利。在SET的AgNiO2专利的2个月前提出申请。并且主张1年前的优先权。 (点击放大) |
虽然专利中的电池在使用锂作为负极这一点上与日后索尼投产的“锂离子电池”相去甚远,但在当时,这些可能阻碍开发进程的专利还是令我们失望至极。
然而,优先权依据的英国专利遍寻不着。在日本国内,他们申请专利的时间也只早了2个月,说不定压根构不成问题,但悬着的心始终放不下来。
 |
| 图5:Goodenough等人在英国临时申请专利的文件 虽然没有正式申请专利,但依然提交了文件,用来主张构想的优先权。英国批准了这样的制度。 (点击放大) |